Il existe de plus en plus de preuves du rôle des cannabinoïdes dans le traitement des maladies neurodégénératives, commotions cérébrales et AVC ischémiques. En plus d’avoir des effets antioxydants et anti-inflammatoires démontrés, les cannabinoïdes s’avèrent également avoir des propriétés neuroprotectrices. Ils pourraient même contribuer à la neurogénèse.
Les effets neuroprotecteurs du cannabis sont principalement mis à profit au niveau médical dans le traitement des maladies neurodégénératives. Ces maladies sont le résultat d’une perte progressive des fonctions des neurones. La maladie de Parkinson se classe au second rang des maladies neurodégénératives développées à l’âge adulte, la plus fréquente étant la maladie d’Alzheimer. Bien que les maladies neurodégéneratives se produisent moins fréquemment chez les enfants, elles existent tout autant, la forme la plus courante étant l’encéphalopathie.
Pour de nombreuses maladies neurodégénératives, l’un des facteurs primaires est généralement une inflammation accompagnée d’une réaction immunitaire entraînant des dommages et un dysfonctionnement des neurones. C’est aussi pour cette raison que de nombreuses maladies neurodégénératives sont développées à l’âge adulte.
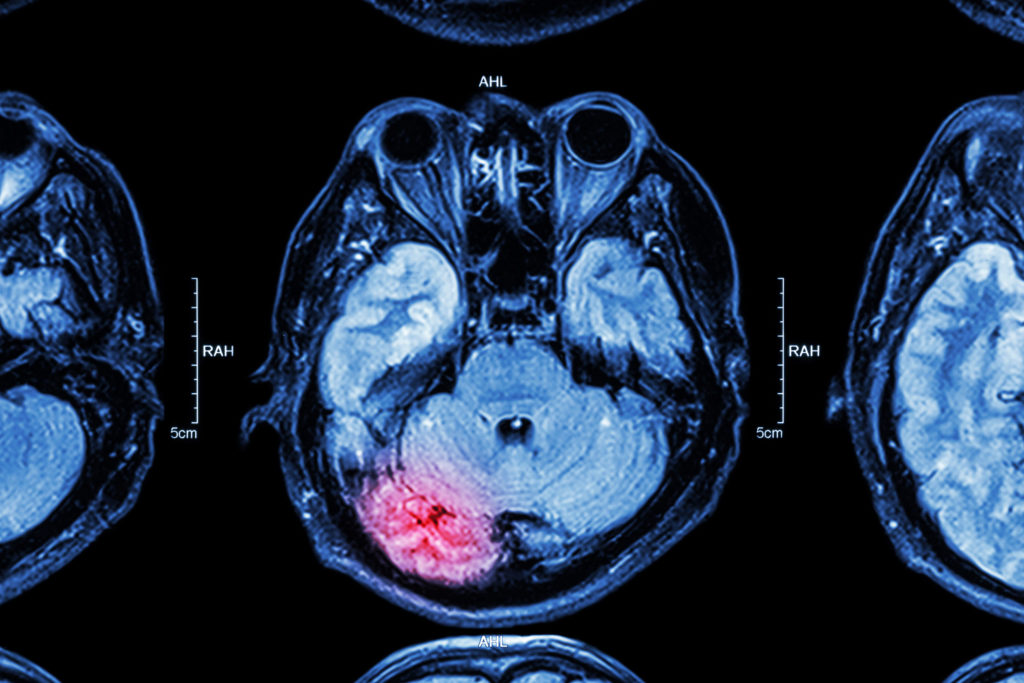
Actuellement, il n’existe pas de traitement pour guérir les maladies neurodégénératives. Au mieux, des médicaments peuvent masquer les symptômes et peut-être stopper la progression de la maladie. C’est là où les effets neuroprotecteurs du cannabis peuvent avoir un rôle à jouer en neurologie.
Le système endocannabinoïde et les maladies neurodégénératives
Les recherches scientifiques menées sur le système endocannabinoïde révèlent de plus en plus d’informations sur leur rôle dans la neuroprotection et les maladies neurodégénératives. Le système endocannabinoïde est un système de signalisation physiologique extrêmement complexe, principalement concentré dans le cerveau. Ce mécanisme humain particulier est d’autant plus intéressant qu’il s’agit d’un système de signalisation qui fonctionne à l’envers.
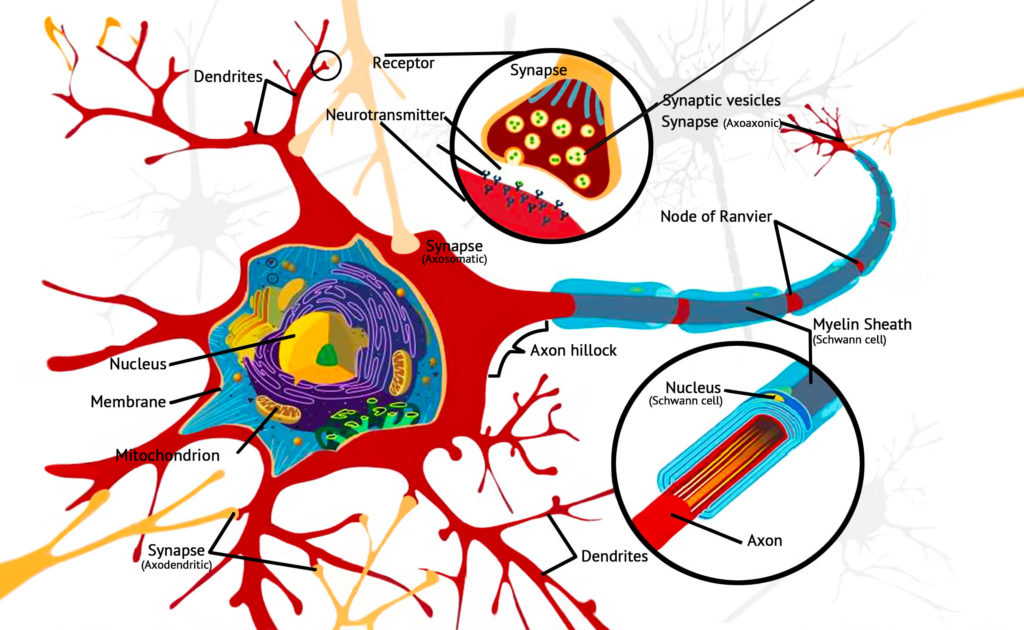
Les cannabinoides endogènes ne sont pas stockés dans les neurones présynaptiques de la même façon que les neurotransmetteurs. Ils sont produits à la demande lorsque la synthèse intracellulaire est déclenchée, le principal facteur déclencheur étant les ions de calcium. C’est l’une des hypothèses selon laquelle le système endocannabinoïde se comporte comme un système de « réparation » ou un mécanisme de guérison de l’organisme.
Les taux d’endocannabinoïdes suite à une lésion cérébrale en sont un exemple approprié. Une étude de 2006 a constaté la présence de taux extrêmement élevés de cannabinoïdes endogènes après des épisodes provoqués par de l’acide kaïnique, une intolérance au glutamate, un stress et un traumatisme dus à un choc. La réaction du système endocannabinoïde à ces événements suggère qu’un des principaux mécanismes compensatoires du cerveau suite à une lésion cérébrale est une signalisation endocannabinoïde.
Ces constatations établissent un lien étroit entre le système endocannabinoïde et une amélioration de la dégénérescence neurologique, et le cannabis constitue par conséquent un objectif thérapeutique potentiel.
Propriétés antioxydantes et anti-inflammatoires du cannabis
Ces dernières années, les propriétés antioxydantes et anti-inflammatoires de divers cannabinoïdes ont été clairement démontrées et nous comprenons mieux le rôle qu’ils jouent dans la modulation de la neurotransmission.
Par conséquent, leur potentiel en tant qu’agents neuroprotecteurs reçoit maintenant toute l’attention qu’il mérite. Il a été démontré que les cannabinoïdes évitent la mort neuronale en cas de lésion neuronale sévère, y compris accident cérébral ischémique et traumatisme cranio-cérébral, et soulagent aussi les symptômes en cas de sclérose en plaques, maladie de Huntington et autres maladies neurodégénératives chroniques.
Les effets antioxydants sont un mécanisme d’action dont on suppose qu’il permet au cannabis de soulager certains symptômes associés à des maladies neurodégénératives. Dès 1998, des chercheurs avaient démontré les effets antioxydants du CBD, remarquant qu’il s’agissait d’un antioxydant plus puissant que l’ascorbate ou les tocophérols, mais sans la toxicité associée à ces composés.
C’est d’autant plus intéressant que le cerveau est l’un des organes les plus vulnérables au stress oxydatif. Le stress oxydatif est essentiellement un déséquilibre dans les réactions d’oxydoréduction, provoquant une quantité excessive de dérivés réactifs de l’oxygène. Certains ont émis l’hypothèse que le stress oxydatif est un facteur crucial dans le déclenchement de la maladie d’Alzheimer. La même chose a été suggérée pour la maladie de Parkinson.
Les propriétés anti-inflammatoires du cannabis peuvent aussi être considérées comme une qualité neuroprotectrice de la plante. On pense que l’activité induite par le récepteur CB2 qui affecte les cellules microgliales réduit les mécanismes neuro-inflammatoires. Dans le contexte actuel de traitement des maladies neurodégénératives, des médicaments anti-inflammatoires sont quelquefois utilisés, spécialement dans le traitement de la maladie d’Alzheimer. Cependant, les études portant sur l’efficacité des anti-inflammatoires utilisés à cette fin ont donné jusqu’ici des résultats très mitigés.
Inhibition des composés provoquant des lésions
Une étude publiée en 2002 (Mechoulam et al) a démontré que la production d’anandamide et de 2-AG augmentait dans le cerveau après un traumatisme cranio-cérébral (TCC). En cas d’un tel traumatisme, certaines substances produites – facteur de nécrose tumorale alpha et dérivés réactifs de l’oxygène (DRO) – sont connues pour provoquer des dommages neuronaux. L’étude a montré que la production d’anandamide et de 2-AG inhibait la présence de ces substances potentiellement néfastes.
Une autre étude menée par Mechoulam s’est intéressée au potentiel inhibiteur du 2-AG et de l’anandamide in vivo. Cette étude a été menée sur des souris et des rats souffrant d’un TCC. Lorsque ces deux composés étaient administrés aux souris et aux rats souffrant d’un TCC, l’étendue de la lésion cérébrale était réduite. Des réductions de l’étendue d’un œdème au cerveau (accumulation de liquide entraînant un gonflement), de l’étendue de l’infarctus (étendue de la nécrose des tissus) et de la mort des cellules de l’hippocampe ont toutes été constatées, ainsi qu’une récupération clinique généralement meilleure.
Cela a un rapport avec le cannabis médical dans la mesure où l’on sait maintenant que le CBD augmente les taux sériques d’anandamide en inhibant les protéines de liaison aux acides gras (FABP), ce qui réduit l’approvisionnement d’anandamide (AEA) à l’hydrolase des amides d’acides gras (FAAH) et perturbe le gradient de concentration vers l’extérieur et vers l’intérieur induit par la FAAH. Il est intéressant de noter que les chercheurs ont aussi démontré que les composés non-cannabinoïdes de cannabis inhibent aussi faiblement la monoacylglycérol lipase , un enzyme responsable de la désintégration du 2-AG.
Les cannabinoïdes dans la récupération après un AVC
Il a été démontré de façon répétée que le THC, le CBD et divers autres cannabinoïdes ont une influence neuroprotectrice pendant et après un AVC ischémique. Alors que diverses études indiquent que la consommation de cannabis peut augmenter le risque d’accident vasculaire, il semble que ce phénomène soit limité à un petit sous-ensemble d’individus prédisposés. Dans 27 % de ces cas, la vasoconstriction cérébrale réversible déclenchée par l’usage de cannabinoïdes peut constituer un mécanisme convaincant d’AVC. Pour la majorité, les thérapies à base de cannabinoïdes se révèlent avoir un potentiel important pour réduire les inflammations et le stress oxydatif dus à un AVC ischémique.
Le CBD a fait l’objet de nombreuses études en tant que neuroprotecteur en cas d’AVC ischémique. Il a été démontré qu’il augmentait le débit sanguin cérébral suite à un AVC ischémique et contribuait par conséquent à réduire le volume de l’infarctus cérébral. Un traitement répété sur 14 jours avec du CBD (10 mg/kg) entraînait une résistance à l’hypothermie et une tolérance aux effets neuroprotecteurs. Pour cette raison, il est considéré comme ayant un plus grand potentiel thérapeutique que le THC dans ce domaine de recherche. Il a aussi été démontré que le CBD réduit l’inflammation causée par la production d’interleukin-1, d’oxyde nitrique et du facteur de nécrose tumorale alpha après un AVC ischémique.
Comme lors d’un TCC, la majeure partie des lésions causées par un AVC sont dues à un stress oxydatif provoqué par l’accumulation de dérivés réactifs de l’oxygène (DRO) en raison d’une activité glutamatergique excessive. Il a été démontré précédemment qu’aussi bien le THC que le CBD sont des antioxydants efficaces qui empêchent la signalisation glutamatergique et réduisent par conséquent l’étendue de l’accumulation de DRO après un AVC ischémique. Cependant, le CBD montre une fois encore une plus grande efficacité en tant qu’antioxydant et a par conséquent un meilleur potentiel thérapeutique que le THC en cas de maladies dégénératives.
Signalisation glutamatergique et cannabinoïdes
Le glutamate est le neurotransmetteur le plus abondant dans le cerveau humain. Ce neurotransmetteur excitateur joue un rôle dans les circuits neuronaux impliqués dans la plasticité synaptique. En renforçant ou en affaiblissant la signalisation entre les neurones, le glutamate joue un rôle vital dans l’apprentissage et la mémoire. On peut dire que c’est le principal neurotransmetteur dans le cerveau, qui détermine comment un individu retient des informations, et c’est un acteur important dans la potentialisation à long terme.
Des niveaux élevés de glutamate provoquent une neurotoxicité (induite en particulier par les récepteurs NMDA, AMPA et récepteurs du glutamate de type kaïnate) et entraînent la formation de composés secondaires causant des lésions telles que DRO et facteur de nécrose tumorale alpha. Il est aussi connu que l’activité du glutamate est réduite par la présence d’antioxydants. Comme il a été démontré que les CBD et THC sont des antioxydants, cela offre une bonne base pour poursuivre les recherches sur les cannabinoïdes dans ce domaine particulier de la neurologie.
Les interactions entre divers cannabinoïdes et le système de signalisation glutamatergique ont été examinées dans une étude intitulée Neuroprotective Antioxidants from Marijuana, (Antioxydants neuroprotecteurs contenus dans la marijuana) publiée en 2000. Dans cette étude, le potentiel neuroprotecteur du cannabidiol et de plusieurs autres cannabinoïdes chez les rats a été examiné in vitro, dans des cultures de neurones exposées à des niveaux toxiques de glutamate. Le CBD a montré les meilleures qualités antioxydantes dans la prévention d’une toxicité au glutamate.
Mécanisme indépendant des récepteurs cannabinoïdes
Les auteurs de Neuroprotective Antioxidants from Marijuana ont également démontré qu’aussi bien le THC que le CBD augmentaient la neuroprotection et réduisaient la neurotoxicité des récepteurs NMDA, AMPA et récepteurs du glutamate de type kaïnate. En outre, le niveau de neuroprotection n’augmentait pas sous l’action d’antagonistes spécifiques des récepteurs cannabinoïdes, indiquant que le mécanisme d’action était indépendant des récepteurs cannabinoïdes.
Des études précédentes avaient conclu que les récepteurs CB2 jouent un rôle dans ces processus cellulaires déterminants. C’est sur cette base que repose l’idée que des agonistes sélectifs de ce type de récepteurs peuvent agir sur les deux aspects du problème en offrant une cytoprotection des cellules nerveuses saines ou en provoquant l’apoptose, c’est-à-dire la mort des cellules tumorales. Cependant, le CBD ne se comporte pas spécifiquement comme un agoniste, par conséquent son potentiel neuroprotecteur doit être réalisé ailleurs.
Il a aussi été démontré que le CBD réduit la toxicité de l’hydropéroxyde (un type de DRO) dans les cultures de cellules de neurones — prouvant encore son efficacité en tant qu’antioxydant. Bien que ces tests aient été effectués in vitro, des études préliminaires in vivo de l’ischémie cérébrale chez les rats suggèrent qu’il est globalement efficace.
Épisode d’hypoxie-ischémie périnatale
Un épisode d’hypoxie-ischémie périnatale est une cause importante de lésion au cerveau au cours de la période néonatale. Il se produit lorsque le flux d’oxygène et de sang vers le cerveau de l’enfant est interrompu en raison d’une asphyxie, souvent au cours de la naissance. Cette pathologie dévastatrice entraîne le décès de 15 à 20 % des enfants diagnostiqués.
Cette pathologie peut aussi entraîner des handicaps neurologiques sévères tels qu’épilepsie, paralysie cérébrale, dysfonctionnement moteur et hyperactivité dans 25 % de cas supplémentaires. Le cerveau en cours de développement est bien plus sensible aux épisodes d’hypoxie-ischémie que le cerveau adulte, dans la mesure où il contient une concentration élevée de vaisseaux sanguins et un volume d’eau plus élevé, et le risque potentiel d’épisodes entraînant des lésions, une hémorragie par exemple, est plus important.
Suivant immédiatement une lésion hypoxique-ischémique au cerveau, une série de mécanismes cellulaires spécifiques, y compris une production accrue de glutamate, est déclenchée, entraînant des dommages cellulaires et menant finalement à une excitotoxicité (un type de mort des cellules causé par une signalisation glutamatergique excessive).
La nature précise de ce processus n’étant pas encore entièrement comprise, en raison de la complexité des mécanismes moléculaires qui sous-tendent la pathologie, on manque d’options efficaces de traitement susceptibles de réduire l’étendue des lésions neuronales. Aujourd’hui cependant, de rapides progrès dans notre compréhension de ce domaine ont suscité un nouveau type de thérapies neuroprotectrices qui doivent être évaluées puis mises en œuvre si leur efficacité est prouvée.
Dans ce cadre, le système endocannabinoïde est à l’étude afin de déterminer son rôle spécifique dans la neuroprotection du cerveau en cours de développement. Alors que l’usage de thérapies cannabinoïdes sur les enfants demeure controversé, suffisamment de succès ont été obtenus avec l’utilisation de cannabinoïdes pour différentes pathologies pédiatriques (y compris épilepsie et cancer) sans effets secondaires négatifs pour que la controverse fasse maintenant rapidement place à un consensus au sein de la communauté scientifique sur les possibilités éventuelles d’application de telles thérapies.
Les cannabinoïdes sont considérés comme de bons candidats pour le traitement des lésions cérébrales périnatales. En plus de moduler les réactions neurales, les cannabinoïdes se sont révélés moduler la vasodilatation due au fonctionnement des cellules endothéliales et de l’activité endothéline, réguler l’homéostasie du calcium et posséder d’importants effets anti-excitotoxiques et anti-inflammatoires.
Il semblerait également que les cannabinoïdes puissent avoir des effets bénéfiques sur la substance blanche, le tissu cérébral composé de fibres nerveuses. Dans cette étude, l’administration de l’agoniste sélectif ACEA du récepteur CB1R au tout début de la période postnatale (du 1er au 14e jour après la naissance) augmente la production de progéniteurs d’oligodendrocytes. La même étude a montré que WIN, un autre cannabinoïde de synthèse, stimulait la myélinisation de la substance blanche sous-corticale.
La recherche semble aussi indiquer le potentiel des endocannabinoïdes à entraîner une réaction réparatrice endogène des neurones. Les agonistes des récepteurs CB tels que le THC doivent être en mesure de stimuler cette réaction endogène.
Les vertus neuroprotectrices du THC pour la population vieillissante
Une étude publiée dans Nature Medicine en 2017 a fait l’objet d’une importante couverture dans les médias en raison de son allégation plutôt inhabituelle, consistant à dire que le THC peut avoir des effets rajeunissants sur le cerveau vieillissant. Même Forbes et The Guardian ont publié des articles sur cette étude.
Dans le cadre de l’essai clinique intitulé « A chronic low dose of Δ9-tetrahydrocannabinol (THC) restores cognitive function in old mice » (Une faible dose régulière de Δ9-tétrahydrocannabinol (THC) rétablit la fonction cognitive chez des souris âgées), les chercheurs ont administré de faibles doses de THC à des souris d’âges divers : 2, 12 et 18 mois, à savoir des souris jeunes, adultes et âgées. Ces doses ont été administrées régulièrement pendant quatre semaines. Le dosage est important dans la mesure où ces doses si minimes n’ont pas d’effets psychotropes tels que ceux entraînés par les dosages utilisés pour un usage récréatif qui sont généralement plus élevés.
Dans l’espace d’un mois, l’équipe dirigée par Andreas Zimmer a évalué la capacité des souris à effectuer des tâches cognitives, par exemple des tests dans un labyrinthe de Morris. L’équipe a observé la capacité des souris à se rappeler où se trouvaient les endroits sans danger ou à reconnaître d’autres sujets de la même espèce auxquels elles avaient été exposées précédemment.
Curieusement, les jeunes souris qui n’avaient pas reçu de faibles doses régulières de THC réalisaient de meilleures performances pour les tests comportementaux de mémoire et d’apprentissage que les jeunes souris qui en en avaient reçu. D’un autre côté, l’inverse était vrai pour les souris âgées : celles qui avaient reçu de faibles doses régulières de THC avaient de meilleurs résultats de tests que les souris adultes et les souris âgées qui n’avaient pas reçu de THC. Les souris ayant reçu régulièrement des faibles doses parvenaient aussi plus rapidement à des résultats.
Cette étude confirme les constatations faites précédemment en utilisant le cannabinoïde de synthèse WIN, où des souris plus âgées démontraient avoir une meilleure mémoire après l’administration de cannabinoïdes. Dans l’étude de 2018 , les souris de sexe féminin âgées de 24 mois avaient reçu une fois une dose de THC de .002mg/kg. Comparées aux souris ayant reçu uniquement le véhicule du médicament, les souris traitées au THC obtenaient de meilleurs résultats dans une batterie de 6 tests de comportement différents. La seule injection de THC augmentait aussi le niveau de Sirtuin1, un enzyme relié à la neuroplasticité à la neuroprotection.
Le déclin cognitif dû au vieillissement n’est pas considéré comme une maladie neurodégénérative, bien qu’il puisse être considéré comme pathologique. Dans la pratique, le seul traitement efficace pour lutter contre le déclin cognitif dû au vieillissement consiste à suivre un régime alimentaire sain, faire de l’exercice et entretenir une activité intellectuelle. Des études sur les rongeurs montrent des résultats extrêmement prometteurs pour le THC utilisé spécifiquement dans le traitement des déficits cognitifs chez la population vieillissante, bien que des études sur des humains soient nécessaires pour confirmer ces résultats.
Un plaidoyer en faveur des acides cannabinoïdes pour la neuroprotection
Cet article s’est surtout intéressé aux phytocannabinoïdes THC et CBD, mais il existe aussi des arguments en faveur des cannabinoïdes sous leur forme acide (THC-A et CBD-A). Ce sont les précurseurs du THC et du CBD, qui existent avant que le processus de décarboxylation se produise. La décarboxylation a pour effet de supprimer le groupe acide carboxyle, transformant par conséquent le THC-A en THC (et le CBD-A en CBD).
Dans cette étude de 2017 publiée dans la revue British Journal of Pharmacology, des chercheurs ont étudié le potentiel de six phytocannabinoïdes différents sur la liaison du récepteur activé par les proliférateurs de peroxysomes PPARγ . Le PPARγ est un type de facteur de transcription des récepteurs nucléaires et est très souvent utilisé dans le traitement du diabète, en raison de sa réaction régulée à l’insuline dans les cellules adipeuses. Cependant, l’activation du PPARγ influence aussi la microglie et par conséquent, a récemment suscité l’attention pour ses possibilités d’application en cas de maladies neuro-inflammatoires chroniques.
L’étude a permis de déterminer que les acides cannabinoïdes lient et activent le PPARγ bien mieux que leurs versions décarboxylées. On a constaté que le THC-A avait une action neuroprotectrice chez les souris, améliorant les déficits moteurs et agissant de façon préventive sur la dégénérescence du striatum.
La forme acide du THC n’est pas psychotrope et constitue par conséquent un cannabinoïde présentant un intérêt médical particulièrement intéressant à étudier. Comme il n’a pas d’effets psychotropes, il peut convenir à une vaste population d’individus, y compris enfants et personnes âgées, qui sont enclins à des maladies neurodégénératives.
Efficacité des cannabinoïdes de synthèse
De même que les endocannabinoïdes et les phytocannabinoïdes, on accorde maintenant de l’attention au potentiel de divers cannabinoïdes de synthèse. Par exemple, dans une étude de 2009 publiée par le Journal of Neuroscience, on a constaté que l’agoniste de synthèse des récepteurs cannabinoïdes R(+)-WIN 55212-2 réduisait in vivo la perte de neurone dans l’hippocampe suite à des ischémies cérébrales chez les rats ainsi que le volume de l’infarctus suite à une ischémie cérébrale focale entraînée par l’occlusion de l’artère cérébrale centrale.
L’énantiomère moins actif (la molécule en image inversée) S(-)-WIN 55212-3 s’est révélée inefficace et l’effet protecteur de R(+)-WIN 55212-2 s’est révélé être bloqué par l’action d’un antagoniste du récepteur CB1 spécifique connu comme « N-(pipéridine-1-yl)-5-(4-chlorophényle)-1-(2,4-dichlorophényle)-4-méthyle-1H-pyrazole-3-carboxamide-hydrochloride ».
Il est intéressant de noter que R(+)-WIN 55212-2 protège aussi les neurones cultivés du cortex cérébral contre une hypoxie et une carence en glucose, mais cet effet était insensible aux antagonistes des récepteurs CB1 et CB2. Il faut des recherches bien plus poussées pour déterminer les interactions précises qui se manifestent ici, mais il est clair qu’il existe un potentiel pour celui-ci et pour d’autres cannabinoïdes de synthèse en tant que traitement de l’ischémie cérébrale, y compris l’AVC.
Les cannabinoïdes ont des propriétés neuroprotectrices démontrées
Il existe de nombreuses preuves de l’efficacité de toute une série de phytocannabinoïdes dans la gestion et l’atténuation des lésions cervicales traumatiques, des AVC ischémiques et du déclin cognitif dû au vieillissement. En outre, nous comprenons de mieux en mieux le rôle que les cannabinoïdes endogènes anandamide et 2-AG jouent dans la modulation de l’inflammation et dans le débit sanguin cérébral. Ce type de recherches ciblent le système endocannabinoïde pour le traitement des maladies neurodégénératives.
Bien qu’il faille mener d’autres études, en particulier sur des sujets humains, les preuves en faveur du rôle des cannabinoïdes dans le traitement des maladies neurodégénératives sont de plus en plus nombreuses. Les mécanismes d’action qui confèrent des propriétés neuroprotectrices aux cannabinoïdes sont vastes, complexes et méritent des recherches plus poussées.
- Disclaimer:Cet article ne remplace aucun conseil, diagnostic ou traitement d’un professionnel médical. Consultez toujours votre médecin ou tout autre professionnel de la santé habilité. Ne tardez pas à obtenir des conseils médicaux et n’ignorez aucune recommandation médicale après avoir lu tout contenu de ce site web.













OÙ apparaissent les commentaires ?? Je serais VOLONTAIRE pour tester certaines expériences afin de faire valider la légalisation totale de plante médicinale ,au moins pour l’usâge médical,mais,à mes CONDITIONS !!….(urgent !!)….
Marijuana users had lower test scores relative to nonusers and showed a significant decline in crystallized intelligence between preadolescence and late adolescence.
extrait de la première étude que vous citer, j’ose pas faire de CC de la seconde, j’comprend pas d’ou sortent toutes vos histoires … combattre la propagande par plus de propagande, c’est vraiment pas ce qui va faire avancer la cause …
Merci pour toutes ces informations Seshata, Dr. Grinspoon, Micha, Sebastián Marincolo et sensiseeds, vos articles sont vraiment complets, intéressants et accessibles à la lecture.
Bien @vous.